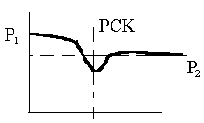
Уравнение процесса дросселирования. Дросселирование идеального
газа.
Дросселирование - падение давления потока жидкости или реального газа и пара в

РСК - называют дросселем.
Что значит резкое ? Несколько формулировок.
Во всех случаях, когда в потоке есть местное сопротивление движению газа или жидкости давление в потоке за сопротивлением меньше, чем до него.
Наличие падения давления сначала было установлено опытным путем. Потом обосновано теретически. В ТД - все основные факты, включая 1-й и 2-й законы были установлены сначала опытным путем.
Рассмотрим поток в трубе с диафрагмой (дросселем)
Рис.
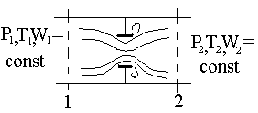
Модель:
-Сечение 1 и 2 трубы до и после Д одинаково-скорости тоже одинаковы w =
w1 = w2-процесс - адиабатный
Тогда общее ур-е 1-го з-на ТД для потока, а оно справедливо для любого потока (в том числе и для потока с трением):
dq = dh + wdw + dl' + gdz + dl'' или для 2-х
q12 - (h2 – h1 ) + (1/2)(w22 – w12 ) + l' + g(z2 – z1 ) + l''
превращается при заданных условиях 1-го и 2-го сечения в очень простое, но важное, мы его уже писали когда разбирали течение в суживающем сопле (но там скорость менялась)
h1 + w2 = h2 + w2
или h1 = h2 ,Что показывает постоянство энтальпии - и обратимого и необратимого горизонтального адиабатного потока малой скорости, не совершающего технической работы.
Для нащего случая дросселирования правильнее писать
h1 = ... = h2 ,
где многоточие отражает, что у нас есть диафрагма
Что происходит в области диафрагмы ?
Из-за сужения (уменьшения сечения):
- w - растет, - кинетическая энергия растет, энтальпия падает а поскольку общее ур-е 1-го з-на ТД
dq = dh - v dp при dq = 0 пишется как dh = v dp
- давление падает - дросселирование !
После диафрагмы поток завихряется, кинетическая энергия затрачивается на работу против сил трения слоев жидкости между собой, при этом выделяется тепло, оно целиком (т.к. процесс адиабатный) воспринимается потоком, его энтальпия возрастает, скорость потока падает.
Значения их во 2-м сечении становятся такими же какими были в 1-м сечении.
Отсюда неизменность энтальпии в потоке в процессе дросселирования.
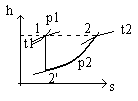
hs – диаграмма
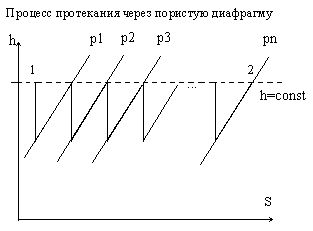
Явление, естественно, проявляется не только в падении давления, но и в изменении других ТД-параметров рассмотрим это.
Процесс дросселирования процесс необратимый. Значит энтропия возрастает.
Применим дифференциальные ур-я ТД. Но сделаем одно важное замечание. ДУ - прменимы только для обратимых процессов. Как быть - подход общий для ТД:
Поскольку s - ф-я состояния, надо подобрать схему обратимого процесса, переводящего РТ из того же 1-го сост. до дросселирования во 2-е - после дросселя.
Изменение s подсчитаем для этого процесса, но поскольку s - ф-я состояния, изменение s в нем отразит то изменение, какое было в процессе дросселирования.
У нас в процессе дросселирования энтальпия 1-го сост. равна энтальпии 2-го. Поэтому примером такого обратимого процесса может быть обратимый процесс расширения c подводом тепла (в нем энтальпия сохраняется)
Тогда:
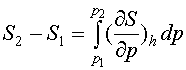
Из 1-го з-на ТД: dh = T ds + v dp (T ds = du + p dv)
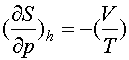
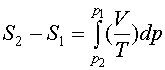
Видно, что энтропия возрастает !
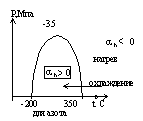
Дросселирование водяного пара.
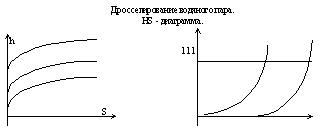 HS - диаграмма.
HS - диаграмма.
Двухфазная смесь при прохождении через дроссель всегда охлаждается. Суть дроссель - эффекта заключается в следующем:
h1 = h2
, тогда U1 + P1V1 = U2 + P2V2Температура растет, когда
U2 > U1, а падает ,когда U2 < U1. Это зависит от соотношений P2V2 и P1V1. При дросселировании всегда P2 < P1. Результат зависит от природы связи частиц рабочего тела. Знак диференциального дроссель-эффекта зависит от изменения параметров межмолекулярных сил.